These AP 9th Physical Science Important Questions and Answers 6th Lesson రసాయన చర్యలు – సమీకరణాలు will help students prepare well for the exams.
AP Board 9th Class Physical Science 6th Lesson Important Questions and Answers రసాయన చర్యలు – సమీకరణాలు
9th Class Physical Science 6th Lesson రసాయన చర్యలు – సమీకరణాలు 1 Mark Important Questions and Answers
ప్రశ్న 1.
Fe2O3+ 2Al → Al2O3 + 2Fe సమీకరణంలో ఏ పదార్ధం ఆక్సీకరణం చెందింది.
జవాబు:
Fe2O3 + 2Al → Al2O3 + 2 Fe ను సమీకరణంలో అల్యూమినియం (Al), Al2O3 గా ఆక్సీకరణం చెందినది.
ప్రశ్న 2.
నీటి సరఫరా కొరకు లోహపు గొట్టాలకు బదులుగా PVC గొట్టాలను ఉపయోగిస్తాము. ఎందుకు?
జవాబు:
PVC పైపులు తుప్పు పట్టవు. కనుక లోహపు గొట్టాలకు బదులుగా PVC గొట్టాలను ఉపయోగిస్తారు.
ప్రశ్న 3.
రసాయన స్థానభ్రంశం అనగానేమి? ఉదాహరణలివ్వంది.
జవాబు:
సమ్మేళనంలో ఒక మూలకం యొక్క స్థానాన్ని, అధిక చర్యాశీలత గల మరొక మూలకం ఆక్రమించటాన్ని రసాయన స్థానభ్రంశం అంటారు.
AB + C → AC + B
- CuSO4 + Zn → ZnSO4 + Cu
- CuSO4 + Fe → FeSO4 + Cu
- 2AgNO3 + Zn → Zn(NO3)2 + 2Ag
ప్రశ్న 4.
ఇనుప వస్తువులను ఆరుబయట తేమగాలిలో ఉంచితే ఏమి జరుగుతుంది? ఆ చర్యను చూపే రసాయన సమీకరణం రాయండి.
జవాబు:
ఇనుప వస్తువులను ఆరుబయట తేమగాలిలో ఉంచిన వాటి ఉపరితలాలపై “తుప్పు” ఏర్పడును.
2Fe(ఘ) + O2(వా) + 4H+(జల) → 2 Fe2+(జల) + 2H2O(ద్ర)
![]()
ప్రశ్న 5.
కాపర్ ఆక్సైడ్ పొడికి హైడ్రోక్లోరిక్ ఆమ్లాన్ని కలిపితే నీలి-ఆకుపచ్చ రంగులో ద్రావణం ఏర్పడింది. ఆ కొత్త పదార్థం ఏమిటో తెలుపండి.
జవాబు:
కాపర్ క్లోరైడ్ (లేక) CuCl2 (or)
Cu0 + 2HCl → CuCl2 + H2O
ప్రశ్న 6.
సమీకరణాన్ని తుల్యం చేయండి.
C3H4 + O2 → 4 CO2 + H2O.
జవాబు:
తుల్యం చేయగా C3H8 + 5O2 → 3CO2 + 4H2O.
ప్రశ్న 7.
సిల్వర్ క్లోరైడ్ సూర్యకాంతి సమక్షంలో వియోగం చెందే రసాయనచర్యకు సమీకరణం రాయంది.
జవాబు:
![]()
ప్రశ్న 8.
ఒక ఇనుప ముక్కను ఘనరూపంలో ఉన్న CuSO4 స్పటికాలలో వేసిన ఏదైనా చర్య జరుగుతుందా? కారణం ఊహించండి.
జవాబు:
ఒక ఇనుప ముక్కను ఘనరూపంలో ఉన్న CuSO4 స్పటికాలలో వేసినప్పుడు రసాయన చర్య జరగదు. కారణమేమనగా CuSO4 స్పటికాలలో Cu+2, SO4-2 అయాన్లు విడివిడిగా ఉండవు. జలద్రావణంలో మాత్రమే అవి అయాన్లుగా ఉంటాయి. కనుక ఇనుము, రాగిని స్థానభ్రంశం చెందించలేదు.
ప్రశ్న 9.
భౌతిక మార్పులు అనగానేమి? ఉదాహరణలివ్వండి.
జవాబు:
రంగులో గానీ, స్థితిలోగానీ, ఉష్ణోగ్రతలో గానీ వచ్చే మార్పులను భౌతిక మార్పులు అంటారు. వీటిని తాత్కాలిక మార్పులు అని కూడా అంటారు.
ఉదా : ఐస్, మైనం కరగటం, నీరు ఆవిరగుట, బల్బు వెలుగుట, ఇనుప ముక్కను అయస్కాంతీకరించుట మొదలైనవి.
ప్రశ్న 10.
తుల్య సమీకరణం అనగానేమి?
జవాబు:
ద్రవ్యనిత్యత్వ నియమం ప్రకారం క్రియాజనకాలలోని పరమాణువుల సంఖ్య, క్రియాజన్యంలోని పరమాణువుల సంఖ్యకు సమానంగా ఉన్న సమీకరణాన్ని ‘తుల్య సమీకరణం’ అంటారు.
ప్రశ్న 11.
రసాయన వియోగాన్ని ఎన్ని రకాలుగా వర్గీకరించవచ్చు?
జవాబు:
రసాయన వియోగాన్ని మూడు రకాలుగా వర్గీకరించవచ్చు. అవి :
- ఉష్ణ వియోగం (Thermal decomposition)
- కాంతి వియోగం (Photolysis)
- విద్యుత్ విశ్లేషణ (Electrolysis)
ప్రశ్న 12.
ఎక్కువ చర్యాశీలత గల లోహాల యొక్క ఆరోహణక్రమాన్ని వ్రాయుము.
జవాబు:
K< Na < Ca < Mg < Al < Zn < Fe < Sn < Pb.
ప్రశ్న 13.
తక్కువ చర్యాశీలతగల లోహాల యొక్క ఆరోహణక్రమాన్ని వ్రాయుము.
జవాబు:
H > Cu > Hg > Ag > Au > PL.
ప్రశ్న 14.
రసాయన స్థానభ్రంశాన్ని చెందించే లోహాలేవి?
జవాబు:
అధిక చర్యాశీలత గల లోహాలు, తక్కువ చర్యాశీలత గల లోహాలను స్థానభ్రంశం చెందించగలవు.
ఉదా :
కాపర్, వెండి, బంగారం, ప్లాటినం లోహాల కంటే అధిక చర్యాశీలత గల హైడ్రోజన్ స్థానభ్రంశం చెందించగలదు.
ప్రశ్న 15.
గాల్వనీకరణం అనగానేమి? (లేక) గాల్వనైజేషన్ అనగానేమి?
జవాబు:
ఇనుప వస్తువులు తుప్పుపట్టకుండా జింక్ లోహంతో పలుచగా పూతగా వేయటాన్ని గాల్వనీకరణం అంటారు. గాల్వనీ కరణం చేసిన గొట్టాలను నీటి సరఫరా కోసం మరియు ఇండ్లకు గేట్లు తయారుచేయటానికి విరివిగా వాడుచున్నారు.
![]()
ప్రశ్న 16.
ర్యాన్సిడిటీ (Rancidity) అనగానేమి?
జవాబు:
నూనెలు లేదా కొవ్వు పదార్థాలు ఎక్కువ కాలం నిల్వ ఉంచడం ద్వారా ఆక్సీకరణం చెంది వాటి రుచిని, వాసనను కోల్పోతాయి. దీనినే ముక్కిపోవటం లేదా ర్యాన్సిడిటీ అంటారు.
ప్రశ్న 17.
ఉష్ణమోచక చర్యలు అనగానేమి? ఉదాహరణలివ్వండి.
జవాబు:
ఒక రసాయన చర్యలో ఉష్ణాన్ని బయటకు విడుదలచేసే చర్యలను ఉష్ణమోచక చర్యలు అంటారు.
ఉదా : శ్వాసక్రియ, మెగ్నీషియం గాలిలో మండటం, ఇంధనాలు దహనం చెందడం మొదలైనవి ఉష్ణమోచక చర్యలు.
i) C + O2 → CO2 + Q (ఉష్ణం)
ii) 2Mg + O2 → 2MgO + O (ఉష్ణం)
iii) CaO + H2O → Ca(OH)2 + Q (ఉష్ణం)
ప్రశ్న 18.
ఉష్ణగ్రాహక చర్యలు అనగానేమి? ఉదాహరణలివ్వండి.
జవాబు:
ఒక రసాయన చర్యలో ఉష్ణాన్ని లోపలకు గ్రహించే చర్యలను ఉష్ణగ్రాహక చర్యలు అంటారు.
ఉదా : 1. N2 + O2 → 2NO – Q (ఉష్ణం)
2. C2H2 + 2H2 → C2H6 – Q (ఉష్ణం)
ప్రశ్న 19.
ఆక్సీకరణం అనగానేమి? ఉదాహరణలివ్వండి.
జవాబు:
ఒక సమ్మేళనానికి ఆక్సిజన్ కలుపుట లేదా హైడ్రోజన్ను తొలగించటాన్ని లేదా ఎలక్ట్రాన్లను కోల్పోవటాన్ని ఆక్సీకరణం అంటారు.
ఉదా : 1. 2Cu + O2 → 2CuO
2. H2S → S + H2 ↑
ప్రశ్న 20.
క్షయకరణం అనగానేమి? ఉదాహరణలివ్వండి.
జవాబు:
ఒక సమ్మేళనానికి హైడ్రోజనను కలుపుట లేదా ఆక్సిజన్ను తొలగించుట లేదా ఎలక్ట్రాన్లను గ్రహించటాన్ని క్షయకరణం అంటారు.
ఉదా : 1. H2 + Br2 → 2HBr
2.2Cu0 → 2Cu + 0,
ప్రశ్న 21.
రెడాక్స్ (ఆక్సీకరణ – క్షయకరణ) చర్యలు అనగానేమి? ఉదాహరణలివ్వంది.
జవాబు:
ఒక రసాయన చర్యలో ఆక్సీకరణం, క్షయకరణం ఒకదాని వెంట మరొకటి జరిగే చర్యలను రెడాక్స్ చర్యలు అంటారు.
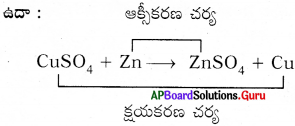
ప్రశ్న 22.
ఆక్సీకరణానికి నిత్యజీవితంలోని అనువర్తనాలేవి?
జవాబు:
ఇనుము తుప్పుపట్టడం, ఆపిల్, బంగాళదుంపలు కోసిన కాసేపటికి రంగు మారటం, కరకరలాడే బిస్కెట్లు, చక్కిలాలు, నూనెలతో చేసే ఆహారపదార్థాలు రుచి, వాసన మారిపోవటం, టపాసులు గాలిలో మండించినపుడు కాంతివంతంగా మండటం మొదలైనవి.
ప్రశ్న 23.
ఇనుప వస్తువులు తుప్పుపట్టడం అనగానేమి ? ఇది ఏ రకమైన చర్య?
జవాబు:
ఇనుప వస్తువులు గాలిలోని తేమ మరియు ఆక్సిజన్తో రసాయన చర్య జరిపి ఆక్సీకరణం చెందటాన్ని తుప్పుపట్టడం అంటారు. ఈ చర్యను ఈ విధంగా చూపవచ్చు. ఇది ఒక సంయోగచర్య.
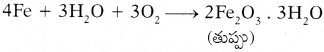
ప్రశ్న 24.
కరోజన్ లేదా క్షయము చెందటం అనగానేమి?
జవాబు:
కొన్ని లోహాలు తేమగాలికి లేదా ఆమ్లాల సమక్షంలో ఉంచినపుడు లోహ ఆక్సైడులను ఏర్పరచటం ద్వారా వాటి మెరుపును కోల్పోతాయి. ఈ చర్యనే క్షయము చెందటం లేదా కరోజన్ అంటారు.
ఉదా : వెండి పై నల్లని పూత, ఇత్తడి, రాగి వస్తువులపై చిలుముపట్టడం.
ప్రశ్న 25.
మిశ్రమ లోహాలు అనగానేమి? ఉదాహరణలివ్వండి.
జవాబు:
రెండు లేదా అంతకన్నా ఎక్కువ లోహాలను తగు నిష్పత్తులలో కలిపినపుడు ప్రత్యేక లక్షణాలు గల క్రొత్త లోహాలు ఏర్పడతాయి. వీటినే మిశ్రమ లోహాలు అంటారు.
ఉదా : స్టెయిన్లెస్ స్టీల్, కంచు, ఇత్తడి, ఉక్కు మొదలైనవి.
ప్రశ్న 26.
ఆపిల్, అరటిపండు, బంగాళదుంప మొదలైనవి కోసిన తర్వాత వాటి రంగు మారును. ఎందువల్ల?
జవాబు:
ఆపిల్, అరటిపండు, బంగాళదుంప మొదలైన వాటితో పాలీఫినాల్ ఆక్సిడేజ్ (లేదా) టైరోసినేజ్ అనే ఎంజైమ్ ఉంటుంది. ఈ ఎంజైమ్ ఆక్సిజన్తో చర్య పొందుతుంది. అందువలన ఆపిల్ వంటి పండ్లను కోసిన తర్వాత ఉపరితలం గోధుమ రంగులోనికి మారుతుంది. దీనిని అరికట్టాలంటే ఆపిల్ ముక్కలను కోసిన వెంటనే నీటిలో ఉంచితే రంగు మారకుండా తాజాగా ఉంటాయి.
ప్రశ్న 27.
రసాయన సమీకరణంలో క్రియాజనకాలు, క్రియాజన్యాలు అనగానేమి?
జవాబు:
ఒక రసాయన చర్యలో ఏ పదార్థాలు రసాయన మార్పుకు గురవుతాయో వాటిని క్రియాజనకాలు’ అని, క్రొత్తగా ఏర్పడిన పదార్థాలను ‘క్రియాజన్యాలు’ అని అంటారు.
ఉదా : 2 ALB, సూర్య కాంతి
![]()
ప్రశ్న 28.
ప్రాథమిక సమీకరణం అనగానేమి?
జవాబు:
అణు ఫార్ములాలు మాత్రమే ఉండే తుల్యం చేయని రసాయన సమీకరణంను ప్రాథమిక సమీకరణం’ అంటారు.
ప్రశ్న 29.
ఉష్ణ వియోగ చర్యలు అనగానేమి? ఒక ఉదాహరణనిమ్ము.
జవాబు:
వేడి చేయుట వలన పదార్థాలు వియోగం చెందినట్లయితే అట్టి చర్యలను ఉష్ణ వియోగ చర్యలు అంటారు.
![]()
ప్రశ్న 30.
కాంతి రసాయన చర్యలు అనగానేమి ? ఉదాహరణనిమ్ము.
జవాబు:
కాంతి సమక్షంలో జరిగే రసాయన చర్యలను కాంతి రసాయన చర్యలు అంటారు.
![]()
ప్రశ్న 31.
ఆక్సీకరణ – క్షయకరణ చర్యలు లేదా రెడాక్స్ చర్యలు అనగానేమి? ఉదాహరణనిమ్ము.
జవాబు:
ఒకే చర్యలో ఆక్సీకరణము, క్షయకరణము జరిగితే అనగా ఒక క్రియాజనకం ఆక్సీకరణం చెందిన మరొక క్రియాజనకం క్షయకరణం చెందుతుంది. ఇటువంటి చర్యలను ‘ఆక్సీకరణ – క్షయకరణ చర్యలు’ లేదా ‘రెడాక్స్ చర్యలు’ అంటారు.
ఉదా : 2 Fe2O3 + 3C → 4 Fe + 3 CO2
ప్రశ్న 32.
వెండి వస్తువులపై నల్లని పూత ఏర్పడుటకు ఒక సమీకరణం వ్రాయుము.
జవాబు:

ప్రశ్న 33.
క్షయము చెందుట (Corrosion) ను ఎలా నివారించవచ్చు?
జవాబు:
క్షయము చెందుట (Corrosion) ను నివారించడానికి లేదా కనీసం తగ్గించడానికి లోహతలంపై ఒక పొరలాంటిది ఏర్పరచి, తద్వారా ఆక్సిజన్ మరియు తేమ తగలకుండా చేస్తారు. లోహతలంపై రంగు వేయడం, నూనె, గ్రీజు లేదా క్రోమియం పూత ద్వారా గాని, మిశ్రమ లోహాలను తయారు చేయడం ద్వారా గాని ఈ సమస్యను నివారిస్తారు.
ప్రశ్న 34.
ముక్కిపోవడం (Rancidity) అనేది ఏ రకమైన చర్య?
జవాబు:
ముక్కిపోవడం (Rancidity) అనేది ఆక్సీకరణ చర్య.
ప్రశ్న 35.
తేమ గల క్లోరిన్ వాయువులు రంగు గల వస్తువులను విరంజనం చెందించుటకు ఒక సమీకరణం రాయుము.
జవాబు:
Cl2 + H2O → HOCl + HCl
HOCl → HCl + (O)
రంగు గల వస్తువు + (O) → రంగు కోల్పోయిన వస్తువు
ప్రశ్న 36.
ఆహారం పాడవకుండా ఉండాలంటే ఏమి చేయాలి?
జవాబు:
ఆహారం పాడవకుండా నిల్వ ఉండాలంటే దానికి విటమిన్ ‘C’ లేదా విటమిన్ ‘E’ లాంటి వాటిని కలపాలి.
ప్రశ్న 37.
సున్నంతో వెల్లవేసిన గోడలు మెరుస్తూ ఉంటాయి. కారణమేమి?
జవాబు:
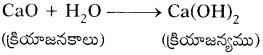
1) పొడి సున్నానికి నీటిని కలపడం ద్వారా తడి సున్నాన్ని తయారుచేస్తారు.
CaO + H2O → Ca(OH)2 + Q
2) ఇలా తయారుచేసిన తడి సున్నాన్ని గోడలకు వెల్ల వేయడానికి వాడతారు.
3) తడి సున్నం (కాల్షియం హైడ్రాక్సైడ్) గాలిలో గల కార్బన్ డై ఆక్సైడ్ (CO2)తో చర్యజరిపి సన్నని, తెల్లని కాల్షియం కార్బొనేట్ పొరను ఏర్పరుస్తుంది. అందువల్లనే సున్నంతో వెల్లవేసిన గోడలు మెరుస్తూ ఉంటాయి.
Ca(OH)2 + CO2 → CaCO3 + H2O
ప్రశ్న 38.
క్రింది సమీకరణములను తుల్యము చేయుము.
a) Na + O2 → Na2O
జవాబు:
4Na + O2 → 2Na2O
b) H2O2 → H2O + O2
జవాబు:
H2O2 → 2H2O + O2
c) Mg(OH)2 + HCl → MgCl2 + H2O
జవాబు:
Mg(OH)2 + 2HCl → MgCl2 + 2H2O
d) Fe + O2 → Fe2O3
జవాబు:
4Fe + 3O2 → 2Fe2O3
ప్రశ్న 39.
క్రింది సమీకరణములను తుల్యము చేయుము.
a) Al(OH)3 → Al2O3 + H2O
జవాబు:
2Al(OH)3 → Al2O3 + 3H2O
b) NH3 + CuO → Cu + N2 + H2O
జవాబు:
2NH3 +3CuO → 3Cu + N2 + 3H2O
c) Al2(SO4)3 + NaOH → Al(OH)3 + Na2SO4
జవాబు:
Al2(SO4)3 + 6NaOH → 2Al(OH)3 + 3Na2SO4
d) HNO3 + Ca(OH)2 → Ca(NO3)2 + H2O
జవాబు:
2HNO3 + Ca(OH)2 → Ca(NO3)2 + 2H2O
e) NaOH + H2SO4 → Na2SO4 + H2O
జవాబు:
2NaOH + H2SO4 → Na2SO4 + 2H2O
f) BaCl2 + H2SO4 → BaSO4 + HCl
జవాబు:
BaCl2 + H2SO4 → BaSO4 + 2HCl
g) Na+H2O → NaOH + H2
జవాబు:
2Na + 24,0 → 2NaOH + H2
h) K2CO3 + HCl → KCl + H2O+ CO2
జవాబు:
K2CO3 + 2HCl → 2KCl + H2O + CO2
![]()
ప్రశ్న 40.
లెడ్ నైట్రేట్ వియోగం చెందడం వలన ఏర్పడే క్రొత్త పదార్థాలు వ్రాయుము.
జవాబు:
లెడ్ ఆక్సైడ్ (PbO), నైట్రోజన్ డై ఆక్సైడ్ (NO) మరియు ఆక్సిజన్ (O2).
ప్రశ్న 41.
ఇనుము త్రుప్పు పట్టడాన్ని నీవు ఏ విధంగా నిరోధిస్తావు?
జవాబు:
రంగు పూయడం, మిశ్రమ లోహాన్ని తయారుచేయడం, గాల్వనైజింగ్ ప్రక్రియల ద్వారా ఇనుము తుప్పుపట్టడాన్ని నివారించవచ్చు.
ప్రశ్న 42.
ఈ క్రింది రసాయన సమీకరణాన్ని తుల్యం చేయంది.
C2H6 O2 → CO2 + H2O
జవాబు:
2C2H6 + 7O2 → 4CO2 + 6H2O
ప్రశ్న 43.
యాంటీ ఆక్సిడెంట్లు అనగానేమి?
జవాబు:
నూనెలు, కొవ్వులు నిల్వ ఉంచడానికి, ఆక్సీకరణం నివారించుటకు కలిపే పదార్థాలను యాంటీ ఆక్సిడెంట్లు అంటారు.
ప్రశ్న 44.
సూర్యకాంతి సమక్షంలో సిల్వర్ బ్రోమైడ్ బూడిద రంగులోనికి మారును. దీనిలో ఇమిడి ఉన్న రసాయన చర్య ఏది?
జవాబు:
కాంతి రసాయన చర్య.
ప్రశ్న 45.
NH4Cl → NH3 + HCl ఇది ఏ రకమైన రసాయనచర్య?
జవాబు:
రసాయన వియోగం.
ప్రశ్న 46.
ఫార్ములా యూనిట్ అనగానేమి?
జవాబు:
అయానిక పదార్థాల ద్రవ్యరాశిని తెలియజేసే విధానాన్ని ఫార్ములా యూనిట్ అంటారు.
ప్రశ్న 47.
ప్రొపేనను (C3H8) ఆక్సిజన్ సమక్షంలో మండించు చర్యకు రసాయన తుల్య సమీకరణం రాయండి.
జవాబు:
C3H8 + 5O2 → 3CO2 + 4H2O
ప్రశ్న 48.
మిశ్రమలోహం అనగానేమి? రెండు ఉదాహరణలిమ్ము.
జవాబు:
ఒక లోహానికి మరొక లోహం లేదా అలోహాన్ని కలపడం ద్వారా ఏర్పడే లోహ మిశ్రమాన్ని మిశ్రమ లోహం అంటారు.
ఉదా : స్టీల్, స్టెయిన్లెస్ స్టీల్.
9th Class Physical Science 6th Lesson రసాయన చర్యలు – సమీకరణాలు 2 Marks Important Questions and Answers
ప్రశ్న 1.
లేత పసుపు రంగు గల సంయోగ పదార్థం ‘X’ ను సూర్యకాంతిలో కొంత సేపు ఉంచాం. అది బూడిదరంగు గల పదారంగా మారింది. ఆ సంయోగ పదార్థం ‘X’ పేరేమిటి? ఇక్కడ జరిగే రసాయనిక చర్య ఏ రకమో ఊహించి, వ్రాయండి.
జవాబు:
1) పసుపు రంగులో ఉన్న ‘X’ అనే పదార్థాన్ని ఎండలో ఉంచినపుడు అది బూడిదరంగులోకి మారింది.
2) అనగా పసుపు రంగులో ఉన్న ‘X’ పదార్థం ‘సిల్వర్ బ్రోమైడ్ (AgBr)” కావచ్చును.
3) దీనిని సూర్యకాంతిలో ఉంచినపుడు బూడిదరంగు గల సిల్వర్ (Ag) మరియు Br (బ్రోమిన్) లుగా వియోగం చెందింది.

ప్రశ్న 2.
క్రింద రసాయన చర్యకు వాటి భౌతిక స్థితులను చూపుతూ సమీకరణాలను వ్రాసి, తుల్యం చేయండి.
బేరియం క్లోరైడ్ మరియు ద్రవ సోడియం సల్ఫేట్ చర్య నొంది బేరియం సల్ఫేట్ అవక్షేపాన్ని మరియు ద్రవ సోడియం క్లోరైడ్ లను ఏర్పరుస్తుంది.
జవాబు:
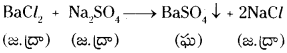
ప్రశ్న 3.
N2(వా) +O2(వా) + ఉష్ణం → 2 NO(వా). ఈ సమీకరణాన్ని బట్టి మీరు ఏమి అవగాహన చేసుకున్నారు? వివరించుము.
జవాబు:
- ఇచ్చిన సమీకరణంలో నైట్రోజన్ వాయువు ఆక్సిజన్ వాయువుతో చర్య జరిపి నైట్రిక్ ఆక్సైడ్ ను ఏర్పరచుచున్నది.
- నైట్రోజన్ ఆక్సీకరణం చెందుతుంది.
- ఇది ఉష్ణగ్రాహక చర్య.
- ఇది రసాయన సంయోగ చర్య.
- ఈ చర్యలో క్రియాజనకాలు, క్రియాజన్యాలు కూడా వాయువులే.
ప్రశ్న 4.
i) CaCO3(ఘ) → CaO(ఘ) + CO2(వా)
ii) 2Ag Br2(ఘ) → 2Ag2(ఘ) + Br2(వా)
పైన తెలిపిన రసాయన చర్యలు ఏరకమైన రసాయన చర్యలో తెలిపి ఇందులో ఏది కాంతి రసాయన చర్యను సూచిస్తుందో తెలుపుము.
జవాబు:
1) ఇచ్చిన రెండు రసాయన చర్యలు రసాయన వియోగ చర్యలే.
2) ఇచ్చిన చర్యలలో కాంతి రసాయన చర్య :
2Ag Br → 2 Ag + Br2
![]()
ప్రశ్న 5.
ఇచ్చిన చర్యలలో ఏర్పడడానికి వీలయ్యే క్రియాజన్యాలను రాయండి. కారణాలను తెల్పండి.
FeCl2 + Zn →
ZnCl2 + Fe →
జవాబు
i) FeCl2 + Zn → ZnCl2 + Fe
ii) ZnCl2 + Fe → ఈ రెండు రసాయనాల మధ్య చర్య జరగదు
కారణం : జింక్ కన్నా ఐరన్ చర్యాశీలత తక్కువ.
ప్రశ్న 6.
క్రింది రసాయన సమీకరణాలను తుల్యం చేయండి.
i) Na + H2O → NaOH + H2
ii) K2CO3 + HCl → KCl + H2O + CO2
జవాబు:
i) 2Na + 2H2O → 2NaOH + H2
ii) K2CO3 + 2HCl → 2KCl + H2O + CO2
ప్రశ్న 7.
కొన్ని లోహాలు ఆక్సిజన్ తో చర్య జరిపి లోహాక్సెడ్లుగా ఆక్సీకరణం చెందుతాయి. ఫలితం అవి పాడైపోతాయి. దీనికి కొన్ని ఉదాహరణలిస్తూ, ఆ చర్యలకు తుల్య సమీకరణాలు వ్రాయండి.
జవాబు:
1. వెండి వస్తువులపై నల్లని పూత ఏర్పడుట.
4 Ag + 2 H2S + O2 → 2 Ag2S + 2H2O
2. రాగి వస్తువులపై ఆకుపచ్చని పూత ఏర్పడుట.
2Cu + O2 → 2 CuO
ప్రశ్న 8.
లోహ క్షయాన్ని నివారించుటకు నీవు సూచించు పద్దతులేవి?
జవాబు:
నివారణలు :
- లోహతలాలపై రంగు వేయుట.
- లోహతలాలపై నూనె, గ్రీజు లేదా క్రోమియం పూత పూయుట ద్వారా.
- మిశ్రమ లోహాలను తయారుచేయుట.
- గాల్వనీకరణం చేయుట మొ||వి.
ప్రశ్న 9.
క్షయం చెందే, క్షయం చెందని లోహాలను ఉదహరించి, కొన్ని లోహాలు క్షయం చెందకపోవడానికి కారణాలు తెల్పండి.
జవాబు:
క్షయం చెందు కొన్ని లోహాలు :
ఇనుము, రాగి, వెండి, మొ||వి.
క్షయం చెందని కొన్ని లోహాలు :
బంగారం మరియు ప్లాటినం.
బంగారం మరియు ప్లాటినములు’ వాతావరణంలోని ఆక్సిజన్, నైట్రోజన్ వంటి ఏ వాయువుతో చర్య జరుపవు. కనుక ఇవి ఏ విధమైన క్షయకరణ స్వభావంను ప్రదర్శించవు.
ప్రశ్న 10.
నీటి సరఫరాకై నీవు సూచించు గొట్టాలు ఏవి? నీ సమాధానాన్ని సమర్థించుము.
జవాబు:
నీటి సరఫరాకై ప్లాస్టిక్ చేసిన PVC పైపులనే నేను సమర్థిస్తాను. ఎందుకనగా ఇనుము, రాగి, జింకుతో చేసిన పైపులు నీటిలోని ఆక్సిజన్, క్లోరిన్, H2 వంటి వాటితో చర్య జరిపి ఆక్సెలను ఏర్పరుస్తాయి. దీని కారణం అవి క్షయము చెందటం జరుగును. అందుకని నేను నీటి సరఫరాకు PVC పైపులను సమర్ధిస్తాను. ఇవి నీటితో, దానిలోని మూలకాలతో ఎట్టి చర్య జరుపవు.
ప్రశ్న 11.
ఇనుము క్షయం చెందే లోహం. దీనిని మిశ్రమలోహంగా మార్చడం ద్వారా లోహక్షయాన్ని అరికట్టవచ్చు. సమర్ధించండి.
జవాబు:
- ఇనుముకు కార్బన్, నికెల్ మరియు క్రోమియం వంటి పదార్థాలను కలపడం ద్వారా “స్టెయిన్లెస్ స్టీల్” అనే మిశ్రమ లోహం ఏర్పడుతుంది. ఈ లోహం గట్టిగా ఉండడంతో పాటు తుప్పు పట్టదు.
- గట్టిగా, దృఢంగా, మెరుస్తూ ఉండేలా కావలసిన లోహ ధర్మాలను అభివృద్ధి చేసుకోవడానికి మిశ్రమ లోహాల తయారీ కూడా చాలా ఉపయోగపడుతుంది.
ప్రశ్న 12.
మీ ఇంటికి నీటి సరఫరాకు నీవు ఏ రకపు గొట్టాలు ఉపయోగిస్తావు?
జవాబు:
- మా ఇంటి నీటి సరఫరా వ్యవస్థలో ఉపయోగించినవి, PVC పైపులు మరియు వాటిని గోడలలో అమర్చుటకు జింకుతో చేసిన క్లాంపులను వాడారు.
- ఇంటిలోని ప్రతి పోరనులోని నీటిని, పంపు వ్యవస్ల యందు కూడా PVC పైపులనే వాడారు.
ప్రశ్న 13.
లోహాలు క్షయం చెందటానికి గాలి, తేమ అవసరమని నిరూపించు ప్రయోగ విధమును వివరించుము.
జవాబు:
సాధారణముగా మనము స్కూలుకి వెళ్ళుటకు వాడు సైకిలును, కొన్ని రోజులు ఆరుబయట ఉంచిన, దానికి ఉండు చైనులు, హ్యాండిల్ మొ||వి వాటిపై ఒక రకపు పొర ఏర్పడును. ఇదియే ఐరన్ ఆక్సెడ్ (తుప్పు). అనగా ఇనుము గాలిలోని తేమ మరియు ఆక్సిజన్లతో చర్య జరిపి ఐరన్ ఆక్సెడు ఏర్పరచినది.
2 Fe + 3O2 + H2O → Fe2O3. H2O
ప్రశ్న 14.
క్రింద ఇవ్వబడిన లోహాలు జాబితాను పరిశీలించి వాటిని క్షయం చెందే, క్షయం చెందని లోహాలుగా వర్గీకరించి పట్టికలో తెల్పండి.
అల్యూమినియం, వెండి, ఇనుము, రాగి, బంగారం, తగరం, టంగ్ స్టన్, ప్లాటినం.
జవాబు:
| క్షయం చెందునవి | క్షయం చెందనివి |
| అల్యూమినియం, వెండి, ఇనుము, రాగి, తగరము, టంగ్స్టన్ | బంగారం, ప్లాటినం |
ప్రశ్న 15.
రసాయన మార్పులు అనగానేమి? ఉదాహరణలివ్వండి.
జవాబు:
శాశ్వత మార్పులను రసాయన మార్పులు అంటారు. రసాయన మార్పులలో కొత్త పదార్థాలు ఏర్పడతాయి. సంఘటనంలో మార్పు వస్తుంది. రసాయన ధర్మాలలో మార్పు వచ్చును.
ఉదా :
ఆహారపదార్థాలను వండుట, పాలు పెరుగుగా మారుట, ఆహారం జీర్ణం అగుట, అగ్గిపుల్ల మండటం, ఇనుము తుప్పుపట్టుట, శ్వాసక్రియ మొదలైనవి.
ప్రశ్న 16.
సాధారణ రసాయన సమీకరణంలో లోపాలేవి?
జవాబు:
సాధారణ రసాయన సమీకరణంలోని లోపాలు :
- క్రియాజనకాల, క్రియాజన్యాల భౌతికస్థితులను తెలియజేయవు.
- చర్య పూర్తి అయినదో, లేదో వివరించదు.
- చర్యా వేగాన్ని వివరించదు.
- చర్యకు అవసరమైన ఉష్ణోగ్రత, పీడనం, ఉత్ప్రేరకాల గురించి వివరించదు.
![]()
ప్రశ్న 17.
కుర్ కురే, లేస్ వంటి ప్యాకెట్లలో నైట్రోజన్ వాయువును ఎందుకు నింపుతారు?
జవాబు:
- నూనెలతో చేసే ఆహార పదార్థాలు గాలిలోని తేమతోనూ, ఆక్సిజన్తోనూ కలిసి ఆక్సీకరణం చెందుతాయి. తద్వారా వాటి తాజాదనాన్ని, కరకరలాడే స్వభావాన్ని కోల్పోతాయి. దీనిని నివారించటానికి కురురే, లేస్ ప్యాకెట్లలో గాలిని తీసివేసి నైట్రోజన్ వాయువును నింపి సీల్ చేస్తారు.
- దీనికి కారణం నైట్రోజన్, జడవాయువుల తర్వాత అతి తక్కువ చర్యాశీలతను కలిగి ఉండును. అందువలన లోపలి ఆహార పదార్థాలతో రసాయన చర్య జరగదు. అందువలన లోపలి పదార్థాలు తాజాగా ఉంటాయి. ఇదే కాకుండా ప్యాకెట్ బయటకు నిండుగా, ఆకర్షణీయంగా ఉంటుంది.
- ఇదే విధంగా విద్యుత్ బల్బులలోనూ ఫిలమెంట్ ఆక్సీకరణం చెందకుండా నైట్రోజన్ వాయువును నింపుతారు.
ప్రశ్న 18.
రసాయన సమీకరణం అనగానేమి ? అందులోని భాగాలేవి?
జవాబు:
- రసాయన చర్యలను అతి సూక్ష్మరూపంలో లేదా సంకేతాలతో తెలియజేస్తే దానిని రసాయన సమీకరణం అంటారు.
- రసాయన సమీకరణంలో ఎడమవైపున సమ్మేళనాలు లేదా మార్పుకు గురి అయ్యే పదార్థాలను క్రియాజనకాలు అంటారు.
- రసాయన సమీకరణంలో కుడివైపున సమ్మేళనాలు లేదా క్రొత్తగా ఏర్పడిన పదార్థాలను క్రియాజన్యాలు అంటారు.
- సమీకరణంలో ‘+’ గుర్తు చర్యని తెలియజేస్తుంది.
- ‘→’ బాణం గుర్తు క్రియాజనకాల నుండి క్రియాజన్యాలు ఏర్పడతాయని తెలియజేస్తుంది.
- ‘↑’ వాయువుని, ‘↓’ అవక్షేపాన్ని తెలియజేస్తుంది.
- B గుర్తు వేడి చేయడాన్ని తెలియజేస్తుంది.
ప్రశ్న 19.
ఒక రసాయన సమీకరణం ఏ విషయాలను తెలియజేస్తుంది?
జవాబు:
ఒక రసాయన సమీకరణం
- చర్యలో పాల్గొన్న క్రియాజనకాలను తెలియజేస్తుంది.
- చర్యలో పాల్గొన్న క్రియాజన్యాలను తెలియజేస్తుంది.
- చర్యలో పాల్గొన్న పరమాణు, అణువుల సంఖ్యలను తెలియజేస్తుంది.
- క్రియాజన్యాల, క్రియాజనకాల అణుభారాలను తెలియజేస్తుంది.
- క్రియాజనకాల, క్రియాజన్యాల మోలుల సంఖ్యను తెలియజేస్తుంది.
- వాయు స్థితిలో ఉన్న క్రియాజనకాల, క్రియాజన్యాల ఘనపరిమాణాలను తెలియజేస్తుంది.
ప్రశ్న 20.
రసాయన సమీకరణాన్ని తుల్యం చేయునపుడు పాటించవలసిన నియమాలేవి?
జవాబు:
- రసాయన సమీకరణాన్ని తుల్యం చేయునపుడు ద్రవ్యనిత్యత్వ నియమం ప్రకారం ఒక చర్యలో పాల్గొన్న పదార్థాల మొత్తం ద్రవ్యరాశి, చర్య ముందు, తరువాత కూడా సమానంగా ఉండాలి.
- ముందుగా రసాయన చర్యలో పాల్గొన్న ప్రతి పదార్థం యొక్క సరియైన సాంకేతికాన్ని రాయాలి.
- సమీకరణాన్ని తుల్యం చేయునపుడు కేవలం గుణకాలను మాత్రమే మార్చాలి. ఫార్ములాను మార్చకూడదు.
- గుణకాలు కనిష్ఠ పూర్ణాంకాలుగా ఉండాలి.
- బాణపు గుర్తుకు ఇరువైపులా మూలక పరమాణువులన్నీ సమానంగా ఉన్నాయో, లేదో సరిచూసుకోవాలి.
ప్రశ్న 21.
రసాయనిక సమీకరణాన్ని ఎలా రాస్తారు?
జవాబు:
- పద సమీకరణ రూపంలో రాసిన రసాయనిక చర్యలో క్రియాజనకాలు క్రియాజన్యాలుగా మారడాన్ని బాణపు గుర్తుతో సూచిస్తాం.
- బాణపు గుర్తుకు ఎడమవైపున క్రియాజనకాలు, కుడివైపున క్రియాజన్యాలు రాస్తాం.
- బాణపు గుర్తు తల క్రియాజన్యాల వైపు ఉంటూ రసాయనిక చర్య దిశను తెలుపుతుంది.
- ఒకవేళ చర్యలో రెండు లేదా ఒకటి కంటే ఎక్కువ క్రియాజనకాలుగాని, క్రియాజన్యాలుగాని ఉన్నట్లయితే వాటి మధ్యలో ‘+’ గుర్తును ఉంచుతాం.
ప్రశ్న 22.
నిత్యజీవితంలో ఆక్సీకరణం యొక్క ప్రభావాలు ఏమిటి?
జవాబు:
- భస్మీకరణం ఆక్సీకరణ ప్రభావాలలో చాలా సాధారణమైనది.
- పిండికి ఈస్టను కలిపి కొద్దిసేపు ఉంచినట్లయితే అది ఉబ్బుతుంది. ఈ చర్యలో చక్కెరలు ఆక్సీకరణం చెంది కార్బన్ డై ఆక్సెడ్, నీరు ఏర్పడుతాయి.
- తేమ గల క్లోరిన్ వాయువులు రంగు గల వస్తువులను విరంజనం చెందించి రంగును కోల్పోయేలా చేస్తాయి.
- కొన్నిసార్లు వర్షాకాలంలో కరెంటు స్థంభం నుండి మన ఇళ్ళకు వచ్చే సరఫరా నిలిచిపోతుంది. దీనికి కారణం విద్యుత్ తీగపై లోహ ఆక్సైడ్ పూత ఏర్పడడమే.
ప్రశ్న 23.
ఒక రసాయన చర్య యొక్క ముఖ్య లక్షణాలేమిటి?
జవాబు:
ఒక రసాయన చర్య యొక్క ముఖ్య లక్షణాలు :
- వాయువులు వెలువడుట
- అవక్షేపం ఏర్పడుట.
- రంగులో మార్పు
- ఉష్ణోగ్రతలో మార్పు
- స్థితిలో మార్పు
ప్రశ్న 24.
నిత్యజీవితంలో కొన్ని రసాయన చర్యలకు ఉదాహరణలివ్వండి.
జవాబు:
- పాలు విరుగుట
- పాలు పెరుగుగా మారుట
- ఆహారం ఉడుకుట
- ఆహారం జీర్ణమగుట
- ద్రాక్ష పళ్ళు పులియుట
- ఇనుము తుప్పుపట్టుట
- ఇంధనాలు మండుట
- కాయలు పళ్ళుగా మారుట
ప్రశ్న 25.
![]()
ఈ సమీకరణమును వివరించుము.
జవాబు:
- ఆక్సిజన్ సమక్షంలో కార్బన్ మండి కార్బన్ డై ఆక్సెడ్ అనే వాయువును వెలువరించును.
- ఈ చర్యలో ఉష్ణం వెలువడినది కావున ఇది ఉష్ణమోచక చర్య.
ప్రశ్న 26.
2Cu + O2 → 2 CuO ఈ సమీకరణం ద్వారా లభించు సమాచారమేమిటి?
జవాబు:
పై సమీకరణం ద్వారా తెలియు విషయాలు :
- రాగి, ఆక్సిజన్ తో చర్య జరిపి కాపర్ ఆక్సెడ్ ను ఏర్పరచును.
- 2 మో ల కాపర్, 1 మోల్ ఆక్సిజన్తో చర్య జరిపి 2 మోల కాపర్ ఆక్సెడు ఏర్పరచును.
ప్రశ్న 27.
ఈ క్రింద తెలుపబడిన సమీకరణము నందలి క్రియాజనకాలు మరియు క్రియాజన్యాలను తెల్పండి.
Na2SO4 + BaCl2 → BaSO4 + 2 NaCl
జవాబు:
1. క్రియాజనకాలు :
సోడియం సల్ఫేట్, బేరియం క్లోరైడ్
2. క్రియాజన్యాలు :
బేరియం సల్ఫేట్, సోడియం క్లోరైడ్
![]()
ప్రశ్న 28.
ఈ క్రింద ఇవ్వబడిన రసాయన సమీకరణాన్ని తుల్యం చేయండి. రసాయన సమీకరణాన్ని తుల్యం చేయడానికి సంబంధించిన సోపానాలను అనుసరించి తుల్యం చేయండి.
Cu2S + O2 → Cu2O + SO2
జవాబు:
Step – 1 : తుల్యం చేయని సమీకరణం ముందుగా వ్రాయాలి.
Cu2S + O2 → Cu2O + SO2
Step – 2 :
గుణకాలను మార్చడం ద్వారా సమీకరణాన్ని తుల్యం చేయడానికి ప్రయత్నం చేయాలి.
2Cu2S + 3O2 → 2Cu2O + 2SO2
Step – 3 :
గుణకాలను కనిష్ఠ పూర్ణాంక రూపంలో మార్చాలి.
Step – 4 :
తుల్యం చేసిన సమీకరణాన్ని వ్రాయాలి.
2Cu2S + 3O2 → 2Cu2O + 2SO2
ప్రశ్న 29.
ఆక్సీకరణ మరియు క్షయకరణల మధ్య భేదాలు తెల్పండి. ఉదాహరణనిమ్ము.
జవాబు:
| ఆక్సీకరణం | క్షయకరణం |
| 1. ఒక సమ్మేళనానికి ఆక్సిజన్ కలపడం లేదా ఒక సమ్మేళనం నుంచి హైడ్రోజన్ తొలగించడం. | 1. ఒక సమ్మేళనానికి హైడ్రోజన్ కలపడం లేదా ఒక సమ్మేళనం నుంచి ఆక్సిజన్ తొలగించడం. |
| 2. ఎలక్ట్రానులు కోల్పోవడం. ఉదా : C + O2 → CO2 |
2. ఎలక్ట్రానులు గ్రహించడం. ఉదా : N2 + 3H2 → 2NH3 |
ప్రశ్న 30.
అవక్షేపాలు ఏర్పడే రసాయన చర్యలను రెండింటిని పేర్కొనండి.
జవాబు:
1) సోడియం సల్ఫేట్ ద్రావణాన్ని, బేరియం ద్రావణాన్ని కలిపితే సోడియం క్లోరైడ్ ద్రావణంతోపాటు తెల్లని బేరియం సల్ఫేట్ అవక్షేపం ఏర్పడుతుంది.
Na2SO4(జ.ద్రా) + BaCl2(జ.ద్రా) → BaSO4(ఘ) ↓ + 2NaCl(జ.ద్రా)
2) సిల్వర్ నైట్రేట్ జలద్రావణం, సోడియం క్లోరైడ్ జలద్రావణంతో చర్య జరిపి సిల్వర్ క్లోరైడ్ అవక్షేపాన్ని ఏర్పరుస్తుంది.
NaCl(జ.ద్రా) + AgNO3(జ.ద్రా) → AgCl(ఘ)+ NaNO3(జ.ద్రా)
ప్రశ్న 31.
40 గ్రాముల మీథేన్ ని దహనం చెందించితే విడుదలయ్యే కార్బన్ డై ఆక్సైడ్ పరిమాణం ఎంత?
జవాబు:

ప్రశ్న 32.
ఫార్ములా యూనిట్ అంటే ఏమిటి? ఉదాహరణలతో వివరించండి.
జవాబు:
ఇచ్చిన ఫార్ములాకు సంబంధించిన ఒక పరమాణువు లేదా అయాన్ లేదా అణువు కావచ్చు.
ఉదా:
- NaCl యొక్క ఫార్ములా యూనిట్, ఒక Na+ అయాన్ మరియు ఒక Cl– అయాన్.
- MgBr2 యొక్క ఫార్ములా యూనిట్, ఒక Mg+ అయాన్ మరియు రెండు Br– అయాన్లు
- H2O ఫార్ములా యూనిట్ ఒక H2O అణువు.
9th Class Physical Science 6th Lesson రసాయన చర్యలు – సమీకరణాలు 4 Marks Important Questions and Answers
ప్రశ్న 1.
క్రింది వాటికి తుల్య రసాయన సమీకరణం రాసి, అవి ఎలాంటి రకమైన చర్యలో తెల్పండి.
A) మెగ్నీషియం(ఘ) + అయోడిన్(వా) → మెగ్నీషియం అయోడైడ్(ఘ)
B) జింక్స్(ఘ) + హైడ్రోక్లోరిక్ ఆమ్లము(జ.ద్రా) → జింక్ క్లోరైడ్(జ.ద్రా) + హైడ్రోజన్(వా)
జవాబు:
Mg + I2 → MgI2
ఇది రసాయన సంయోగ చర్య.
Zn + 2HCl → ZnCl2 + H2 ↑
ఇది రసాయన స్థానభ్రంశ చర్య.
ప్రశ్న 2.
రసాయన సమీకరణాలను ఎందుకు తుల్యం చేయాలి? ఏదైనా ఒక రసాయన సమీకరణాన్ని తీసుకొని తుల్యం చేసే విధానాన్ని వివరించండి.
జవాబు:
ఏ సమీకరణంలో అయితే క్రియాజనకాల వైపుగల మూలక పరమాణువుల సంఖ్య, క్రియాజన్యాల వైపు గల మూలక పరమాణువుల సంఖ్యకు సమానంగా ఉంటుందో అటువంటి సమీకరణాన్ని తుల్య సమీకరణం అంటారు.
ఒక రసాయన చర్యలో పరమాణువులు సృష్టించబడవు, లేదా నాశనం చెయ్యబడవు. అనగా చర్యకు ముందు మరియు చర్య జరిగిన తరువాత మూలక పరమాణువుల సంఖ్య సమానంగా ఉండాలి. దీనినే ద్రవ్యనిత్యత్వ నియమం అంటారు.
కాబట్టి ఒక రసాయన సమీకరణం ఖచ్చితంగా తుల్యం చేయబడాలి.
ఉదా : 2H, + 0, 28,0
ప్రశ్న 3.
క్రింది రసాయన సమీకరణాలను తుల్యం చేయుము.

జవాబు:

ప్రశ్న 4.
నీటి రసాయన వియోగం (నీటి విద్యుత్ విశ్లేషణ) ప్రయోగాన్ని నిర్వహించుటకు కావలసిన పరికరాల జాబితా రాయంది. ప్రయోగ విధానాన్ని వివరించండి. ఈ చర్యలో ఏర్పడే క్రియాజన్యాలను తెల్పండి.
జవాబు:
కావలసిన పరికరాలు :
ప్లాస్టిక్ మగ్గు / బీకర్, రెండు పరీక్ష నాళికలు, 9V బ్యాటరీ, స్విచ్, రెండు గ్రాఫైట్ ఎలక్ట్రోడ్లు , వాహక తీగలు, నీరు.
ప్రయోగ విధానము:
i) ఒక ప్లాస్టిక్ మగ్గును / బీకర్ను తీసుకుని దాని అడుగు భాగంలో రెండు రంధ్రములను చేసి, ఎలక్ట్రోడ్లను అమర్చాలి.
ii) మగ్గులో / బీకరులో ఆమీకృత నీటిని పోసి రెండు పరీక్ష నాళికలనూ నీటితో నింపి రెండు ఎలక్ట్రోడ్లపై తలక్రిందులుగా బోర్లించాలి.
iii) ఎలక్ట్రోడ్లను స్విచ్, బ్యాటరీల ద్వారా వలయం పూర్తి చేసి నీటిలో విద్యుత్ ప్రవహింపచేయాలి.
iv) పరీక్షనాళికలలో వాయువులు వెలువడుటను గమనించాలి.
క్రియాజన్యాలు :
హైడ్రోజన్, ఆక్సిజన్లు.
![]()
ప్రశ్న 5.
జింక్, హైడ్రోక్లోరిక్ ఆమ్లం మధ్య జరిగే చర్యకు సమీకరణం రాని తుల్యం చేయండి. ఈ చర్యలో 1 మోల్ HCl పూర్తిగా పాల్గొంటే S.T.P. వద్ద విడుదలయ్యే హైడ్రోజన్ వాయువులోని అణువుల సంఖ్యని లెక్కించండి.
[గ్రామ్ మోలార్ ఘనపరిమాణం = 22.4 లీ. (S.T.P. వద్ద) అవగాడ్రో సంఖ్య = 6.023 × 1023]
జవాబు:
Zn + 2HCl → ZnCl2 + H2 చర్యలో 2 మో HCI పూర్తిగా పాల్గొంటే 1 మోల్ హైడ్రోజన్ వాయువు విడుదలవుతుంది. కాబట్టి 1 మోల్ HCI పూర్తిగా పాల్గొంటే ½ మోల్ హైడ్రోజన్ వాయువు వెలువడుతుంది.
ఒక మోల్ H2 వాయువులో ఉండే H2 అణువుల సంఖ్య 6.023 × 1023
½ మోల్ H, వాయువులో ఉండే H, అణువుల సంఖ్య = 6.02 × 1023 × ½ = 3.011 × 1023
ప్రశ్న 6.
మిశ్రమ లోహంగా మార్చడం ద్వారా లోహక్షయం నివారించబడుతుంది. దీని సమర్థనకు నీవు అడిగే ప్రశ్నలు ఏవి?
జవాబు:
- లోహాలను మిశ్రమముగా చేయుటకు ఏ లోహాలను కలపాలి?
- మిశ్రమాలుగా వాడు లోహాల పేర్లేవి?
- అన్ని లోహాలనూ కలిపి మిశ్రమాలు అంటారా? ఎందుకు?
- ఈ మిశ్రమ లోహం ధృడంగా ఉంటుందా?
- ఈ మిశ్రమ లోహం కాంతిని (మెరుపు) ను కోల్పోదా?
- లోహం – లోహంతోనే మిశ్రమం చెందాలా? అలోహంతో కూడా మిశ్రమం చెందవచ్చా?
- సాధారణ లోహం, మిశ్రమ లోహంలు చేసే రసాయన చర్యలో ఏ రకమైన తేడా కలదు?
- మిశ్రమలోహం, ప్రధానలోహం యొక్క లోహధర్మంను అభివృద్ధి పరచునా?
ప్రశ్న 7.
కాల్షియం నైట్రేట్ పై ఉష్ణం యొక్క చర్యను చూపే క్రింది రసాయన సమీకరణాన్ని పరిశీలించండి.
2Ca (NO3)2 → Ca0 + 4NO2 ↑ + O2 ↑
జవాబు:
ఇవ్వబడిన తుల్య సమీకరణము
![]()
ఇక్కడ Ca ((NO3)2, CaO ల అణుద్రవ్యరాశులు వరుసగా 164 మరియు 56,
అ) ఒక మోల్ 2 Ca (NO3)2 వియోగం చెందినపుడు ఎన్ని మోల్ NO2 ఏర్పడుతుంది?
జవాబు:
పై తుల్య సమీకరణముననుసరించి ఒక మోల్ 2 Ca (NO3)2 వియోగం చెందినపుడు 4 మోe NO2 ఏర్పడును.
ఆ) స్థిర ఉష్ణోగ్రతా పీడనాల వద్ద 164 గ్రాముల Ca (NO3)2 వేడిచేసినపుడు ఉత్పత్తి అయ్యే NO2 ఘనపరిమాణం ఎంత?
జవాబు:
Ca (NO3)2 యొక్క అణుభారము = 164 గ్రాములు
స్థిర ఉష్ణోగ్రతా పీడనాల వద్ద 2 × 164 గ్రాములు Ca (NO3)2లను వేడి చేసినపుడు 22.4 × 4 లీటర్ల NO2 ను విడుదల చేయును. అదే ఉష్ణోగ్రతా పీడనాల వద్ద 164 గ్రాముల Ca (NO3)2 ను వేడిచేసినపుడు విడుదలగు
![]()
ఇ) 82 గ్రాముల Ca (NO3)2 ను వేడిచేసినపుడు ఏర్పడే కాల్షియం ఆక్సెడ్ ద్రవ్యరాశిని లెక్కించంది.
జవాబు:
తుల్య సమీకరణం నుండి 164 గ్రాముల Ca (NO3)2 వియోగం చెంది 112 గ్రాముల CaO ను ఏర్పరచును.
అదే 82 గ్రాముల Ca (NO3)2 వియోగం చెంది విడుదలచేయు Ca0 విలువ = [latex]\frac{82}{164}[/latex] × 112 = 56 గ్రాములు
ఈ) 5 మోల్ O2 క్రియాజన్యాలను ఉత్పత్తి చేయడానికి అవసరమైన Ca (NO3)2 పరిమాణం ఎంత?
జవాబు:
పై తుల్య సమీకరణం నుండి 2 మోల్ Ca (NO3)2, 5 మోల్ల వాయువులు (4 మోల్ల NO2 మరియు 1 మోల్ ఆక్సిజన్)ను విడుదల చేయుచున్నవి.
5 మోల్ల వాయు ఉత్పన్నాలు ఏర్పడాలంటే కావలసిన Ca (NO3)2 ద్రవ్యరాశి = 2 × 164 = 328V
ప్రశ్న 8.
ఒక విద్యార్థికి కింది పదార్థాలను ఇచ్చి రసాయన చర్యా రకాలను ప్రయోగం చేసి చూపమన్నారు. అతడు ఏ విధంగా చేసి ఉంటాడో రాయండి.
కాపర్ సల్ఫేట్ ద్రావణం, బేరియం క్లోరైడ్ ద్రావణం, ఫెర్రస్ సల్ఫేట్ స్ఫటికాలు, ఇనుప మేకులు, పొడిసున్నం, నీరు.
జవాబు:
విద్యార్థికి ఇచ్చిన పదార్థాలు :
CuSO2 ద్రావణం, BaCl2 ద్రావణం, ఇనుప మేకులు (Fe), ఫెర్రస్ సల్ఫేట్ (FeSO4), పొడిసున్నం (CaO) మరియు నీరు (H2O).
1. కాపర్ సల్ఫేట్ ద్రావణం :
కాపర్ సల్ఫేట్ ద్రావణంలో, జింక్ ముక్కలను కలిపిన కాపర్ కంటే జింకుకు చర్యాశీలత ఎక్కువ కనుక, జింకు, కాపర్ను దాని స్థానం నుండి స్థానభ్రంశం చెందించును. కనుక ఇది ఒక రసాయన స్థానభ్రంశ చర్య.
CuSO4 + Zn → ZnSO4 + Cu
2. బేరియం క్లోరైడ్ ద్రావణం :
బేరియం క్లోరైడ్ ను ఫెర్రస్ సల్ఫేట్ ద్రావణంతో చర్య జరిపితే రసాయన ద్వంద్వ వియోగం జరిగి BaSO4 మరియు FeCl2, ఏర్పడును.
BaCl2(జల) + FeSO4(జల) → BaSO4(ఘ) ↓ + FeCl2(జల)
3. ఇనుప మేకులు (Fe) :
కాపర్ సల్ఫేట్ లో ఇనుపమేకులను ముంచిన అవి గోధుమరంగులోకి మారును. CuSO4 రంగును కోల్పోవును. ఇది ఒక స్థానభ్రంశ చర్య.
Fe(ఘ) + CuSO4(జల) → FeSO4(జల) + Cu(ఘ)↓
4. ఫెర్రస్ సల్ఫేట్ స్ఫటికాలు :
ఫెర్రస్ సల్ఫేట్ స్ఫటికాలను వేడిచేసిన, అవి వియోగము చెంది Fe2O3, SO2, SO3 లు ఏర్పడును.
![]()
5. పొడిసున్నం :
పొడిసున్నంను నీటితో చర్యజరిపిన తడిసున్నం ఏర్పడును. CaO(ఘ) + H2O(ద్ర) → Ca (OH)2(జల)
6. నీరు :
నీటిని విద్యుత్ విశ్లేషణం చెందించిన అది హైడ్రోజన్ మరియు ఆక్సిజన్లుగా విడిపోవును.
![]()
ప్రశ్న 9.
రసాయన సమీకరణం ద్వారా అదనపు సమాచారాన్ని ఎలా తెలుసుకోవచ్చు?
జవాబు:
రసాయన సమీకరణాల ద్వారా మరింత సమాచారం తెలుసుకోవడానికి క్రియాజనకాలు, క్రియాజన్యాలకు సంబంధించిన కింద సూచించిన లక్షణాలు తెలియజేయడం ఎంతగానో ఉపయోగపడుతుంది.
i) భౌతిక స్థితి
ii) ఉష్ణోగ్రతలో మార్పులు (ఉష్ణమోచక లేదా ఉష్ణగ్రాహక చర్యలు)
iii) ఏదైనా వాయువు వెలువడడం
iv) ఏదైనా అవక్షేపం ఏర్పడడం
i) భౌతిక స్థితిని తెలియజేయుట :
పదార్థాలు ప్రధానంగా ఘన, ద్రవ, వాయు స్థితులలో ఉంటాయి. వీటిని వరుసగా (ఘ), (ద్ర), (వా) లాంటి గుర్తులతో రసాయన సమీకరణాలలో సూచిస్తారు. ఏదైనా పదార్థం నీటిలో కరిగి ఉన్నట్లయితే వాటిని జల ద్రావణాలు (జ.ద్రా. )తో సూచిస్తారు.
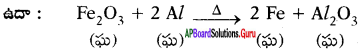
ii) ఉష్ణ మార్పులను తెలియజేయుట :
ఉష్ణాన్ని విడుదల చేస్తే జరిగే చర్యలను ఉష్ణమోచక చర్యలని, ఉష్టాన్ని గ్రహిస్తూ జరిగే చర్యలను ఉష్ణగ్రాహక చర్యలు అని అంటారు.
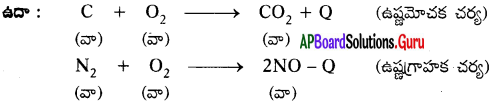
iii) వాయువు విడుదలను సూచించుట :
ఒక రసాయనిక చర్యలో వాయువు విడుదలైతే, దానిని పైకి చూపిస్తున్న బాణపు గుర్తు (↑) తో సూచిస్తాం.

iv) అవక్షేపం ఏర్పడడాన్ని సూచించుట :
ఒక రసాయనిక చర్యలో అవక్షేపం ఏర్పడితే, దానిని క్రిందవైపుకు సూచిస్తున్న బాణపు గుర్తు (↓) తో సూచిస్తాం.
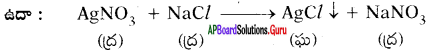
ప్రశ్న 10.
రసాయన చర్యలు ఎన్ని రకములు? అవి ఏవి? ఉదాహరణలతో వివరింపుము.
జవాబు:
రసాయన చర్యలు నాలుగు రకాలు. అవి:
1. రసాయన సంయోగం : రెండు లేదా అంతకన్నా ఎక్కువ పదార్థాలు కలిసి ఒక క్రొత్త పదార్ధంగా ఏర్పడటాన్ని రసాయన సంయోగం అంటారు.
ఉదా : 2Mg + O2 → 2MgO
2. రసాయన వియోగం :
ఒక సమ్మేళనం శక్తి సమక్షంలో రెండు కాని అంతకంటే ఎక్కువ పదార్థాలుగా విడిపోవడాన్ని రసాయన వియోగం అంటారు.
![]()
3. రసాయన స్థానభ్రంశం :
సమ్మేళనంలోని ఒక మూలకం యొక్క స్థానాన్ని, అధిక చర్యాశీలత గల మరొక మూలకం ఆక్రమించడాన్ని రసాయన స్థానభ్రంశం అంటారు.
ఉదా : Zn + CuSO4 → ZnSO4 + Cu
4. రసాయన ద్వంద్వ వియోగం :
రెండు క్రియాజనకాలు తమ ప్రాతిపదికలను పరస్పరం మార్పిడి చేసుకొనే రసాయన చర్యను రసాయన ద్వంద్వ వియోగం అంటారు.

ప్రశ్న 11.
రెండు బీకర్లను తీసుకొని వాటిలో లెడ్ నైట్రేట్ జల ద్రావణం మరియు పొటాషియం అయోడైడ్ జల ద్రావణాలను తయారుచేస్తే అవి ఏ రంగులో ఉంటాయి? ఆ రెండు ద్రావణాలను వేరొక బీకరులో కలిపితే ఏమి జరుగుతుంది? ఇది ఏ రకమైన రసాయన చర్య? ఏర్పడే క్రియాజన్యాలను తెల్పుము.
జవాబు:
రెండు ద్రావణాలు తెల్లరంగులోనే ఉంటాయి. ఆ రెండు ద్రావణాలను కలిపితే పసుపురంగు అవక్షేపం ఏర్పడుతుంది. ఇది రసాయన ద్వంద్వ వియోగ (అవక్షేప) చర్య. రెండు ద్రావణాల మధ్య చర్య జరిగి లెడ్ అయోడైడ్ అవక్షేపం (పసుపురంగు) ఏర్పడుతుంది. పొటాషియం నైట్రేట్ ద్రావణంలో ఉంటుంది. .
Pb(NO3)2 + 2KI → PbI2 + 2KNO3
![]()
ప్రశ్న 12.
లత కొంత పరిమాణంలో ఒక పదార్థ చూర్ణాన్ని పరీక్షనాళికలోనికి తీసుకొంది. స్పిరిట్ ల్యాంతో దానిని వేడిచేసింది. వెలువడిన వాయువును రెండవ పరీక్షనాళికలో ఉన్న ద్రావణంలోనికి పంపింది. రెండవ పరీక్ష నాళికలో ద్రావణం పాలవంటి తెల్లని రంగులోకి మారింది. ఈ క్రింది ప్రశ్నలకు సమాధానమిమ్ము.
ఎ) వేడిచేయబడిన పదార్థం ఏమై ఉంటుంది?
బి) వెలువడిన వాయువు ఏమిటి?
సి) రెండవ పరీక్షనాళికలో తీసుకొన్న ద్రావణం ఏమిటి?
డి) ఈ ప్రయోగంలో ఏ రకపు రసాయనచర్యలు ఇమిడి ఉన్నాయి?
జవాబు:
ఎ) వేడిచేయబడిన పదార్థం కాల్షియం కార్బొనేట్ (మరి ఏదైనా లోహ కార్బొనేట్ కావచ్చు).
బి) వెలువడిన వాయువు కార్బన్ డై ఆక్సైడ్,
సి) సున్నపుతేట లేదా తడిసున్నం (Ca(OH)2).
డి) ఈ ప్రయోగంలో వియోగ చర్య మరియు తటస్థీకరణ చర్యలు ఇమిడి ఉన్నాయి.
CaCO3 → CaO + CO2 (రసాయన వియోగ చర్య)
Ca(OH)2 + CO2 → CaCO3 + H2O (తటస్థీకరణ చర్య)
ప్రశ్న 13.
కొంత పరిమాణంలో లేత పసుపు రంగు గల ఒక పదార్థాన్ని వాచ్ గ్లాస్ నందు తీసుకొని, దానిని కొంతసేపు ఎండలో ఉంచారు. అది బూడిదరంగు గల చూర్ణంగా మారింది.
ఎ) లేత పసుపు రంగుగల పదార్థం ఏమిటి?
జవాబు:
సిల్వర్ బ్రోమైడ్
బి) బూడిద రంగులో ఏర్పడిన క్రొత్త పదార్థం ఏమిటి?
జవాబు:
సిల్వర్
సి) ఇది ఏ రకమైన రసాయన చర్య?
జవాబు:
కాంతి రసాయన చర్య (రసాయన వియోగం)
డి) ఈ రసాయన చర్యకు రసాయన సమీకరణం వ్రాయుము.
జవాబు:
2AgBr(ఘ) → 2Ag(ఘ) + Br2(ఘ)
ప్రశ్న 14.
ఈ క్రింది సమీకరణాలకు తుల్య సమీకరణాలు వ్రాయుము.
ఎ) Na2SO4 + BaCl2 → BaSO4 + NaCl
బి) Al4C3 + H2O → CH4 + Al(OH)3
సి) Pb(NO3)2 → PbO + NO2 + O2
డి) Fe2O3 + Al → Al2O3 + Fe
జవాబు:
ఎ) Na2SO4 + BaCl2 → BaSO4 + NaCl
Na2SO4 + BaCl2 → BaSO4 + 2NaCl
బి) Al4C3 + H2O → CH4 + Al (OH)3
Al4C3 + 12H2O → 3CH4 + 4Al (OH)3
సి) Pb(NO3)2 → PbO + NO2 + O2
2Pb(NO3)2 → 2PbO + 4NO2 + O2
డి) Fe2O3 + Al → Al2O3 + Fe
Fe2O3 + 2Al → Al2O3 + 2 Fe
ప్రశ్న 15.
నిత్యజీవిత ఆక్సీకరణ చర్యలకు ఏవేని ‘8’ ఉదాహరణలిమ్ము.
జవాబు:
నిత్యజీవితంలో ఆక్సీకరణ చర్యలు :
- ఆహారం ముక్కిపోవడం
- ఇనుము తుప్పుపట్టడం
- ఇంధనాలను మండించడం
- ఆపిల్ ను కోసినపుడు అది గోధుమరంగులోకి మారడం
- టపాసులు పేలడం
- రంగు గల వస్తువులు ఆక్సీకరణం చెంది వాటి రంగును కోల్పోతాయి.
- పిండికి ఈస్టు కలిపితే అది ఉబ్బుతుంది. ఈ చర్యలో చక్కెరలు ఆక్సీకరణం చెంది కార్బన్ డై ఆక్సైడ్, నీరు ఏర్పడుతుంది.
- వెండి, రాగి వస్తువులపై రంగుపూత (చిలుము) ఏర్పడటం,
ప్రశ్న 16.
మీ మిత్రునికి/మిత్రురాలికి రసాయన ద్వంద్వ వియోగం అనే అంశం గురించి కొన్ని సందేహాలున్నాయి. దానిని నివృత్తి చేయుటకు నీవు ఎటువంటి ప్రయోగాలు చేసి చూపిస్తావు? వివరింపుము.
జవాబు:
రసాయన ద్వంద్వ వియోగానికి సంబంధించి చేసే ప్రయోగాలు:
1) లెడ్ నైట్రేట్ ద్రావణానికి పొటాషియం అయోడైడ్ ద్రావణం కలిపితే పసుపురంగు అవక్షేపం లెడ్ అయోడైడ్ మరియు ద్రావణంలో పొటాషియం నైట్రేట్ ఏర్పడతాయి.
ఈ చర్యలు లెడ్ అయాన్ మరియు పొటాషియం అయాన్ వాటి స్థానాలు పరస్పరం మార్చుకొంటాయి.
Pb (NO3)2(జ.ద్రా) + 2KI(జ.ద్రా) → Pbl2(ఘ) + 2KNO3(జ.ద్రా)
2) సోడియం సల్ఫేట్ ద్రావణానికి బేరియం క్లోరైడ్ ద్రావణాన్ని కలిపితే సోడియం క్లోరైడ్ ద్రావణంతోపాటు తెల్లని బేరియం సల్ఫేట్ అవక్షేపం ఏర్పడుతుంది.
Na2SO4(జ.ద్రా) + BaCl2(జ.ద్రా) → BaSO4(ఘ) + 2Nacl(జ.ద్రా)
సోడియం, బేరియం అయాన్లు పరస్పరం తమ స్థానాలను మార్చుకొన్నాయి.
3) సోడియం హైడ్రాక్సైడ్, హైడ్రోక్లోరిక్ ఆమ్లంతో చర్యజరిపి సోడియం క్లోరైడ్ మరియు నీరు ఏర్పరుస్తుంది.
NaOH(జ.ద్రా) + HCl(జ.ద్రా) → NaCl(జ.ద్రా) + H2O(ద్ర)
Na+ H+ అయాన్లు తమ స్థానాలను మార్చుకొన్నాయి.
4) సిల్వర్ నైట్రేట్ జలద్రావణంకు సోడియం క్లోరైడ్ ద్రావణాన్ని కలిపితే సిల్వర్ క్లోరైడ్ అవక్షేపం ఏర్పడుతుంది.
AgNO3(జ.ద్రా) + NaCl(జ.ద్రా) → AgCl(ఘ) + NaNO3(జ.ద్రా)
Ag+, Na+ లు తమ స్థానాలను పరస్పరం మార్చుకొన్నాయి.
9th Class Physical Science 6th Lesson రసాయన చర్యలు – సమీకరణాలు 1 Mark Bits Questions and Answers
సరియైన సమాధానమును గుర్తించండి.
1. C6H12O6 → C2H5OH + CO2 అనే చర్య
A) సంయోగం
B) వియోగం
C) స్థానభ్రంశం
D) ద్వంద్వ వియోగం
జవాబు:
B) వియోగం
2. BaCl2 + Na2SO4 → BaSO4 + 2NaCI అనే సమీకరణం ఈ రకం చర్యను సూచిస్తుంది.
A) స్థానభ్రంశం
B) వియోగం
C) సంయోగం
D) ద్వంద్వ వియోగం
జవాబు:
D) ద్వంద్వ వియోగం
![]()
3. నీటి విద్యుత్ విశ్లేషణ ప్రయోగంలో విడుదలయ్యే ఆక్సిజన్, హైడ్రోజన్ వాయువుల ఘనపరిమాణాల నిష్పత్తి …..
A) 1 : 2
B) 2 : 1
C) 1 : 1
D) 3 : 1
జవాబు:
A) 1 : 2
4. కాపర్ సల్ఫేట్ ద్రావణంలో ముంచిన ఇనుపమేకు గోధుమ రంగులోకి మారి నీలిరంగు కాపర్ సల్ఫేట్ ద్రావణం రంగు కోల్పోవును. ఇది ఎటువంటి రసాయన చర్య?
A) రసాయన సంయోగం
B) రసాయన వియోగం
C) రసాయన ద్వంద్వ వియోగం
D) రసాయన స్థానభ్రంశం
జవాబు:
D) రసాయన స్థానభ్రంశం
5. x KClO3 → yKCl + zO2 సమీకరణంలో x, y, z విలువలు వరుసగా
A) 1, 2, 3
B) 3, 3, 2
C) 2, 2, 3
D) 2, 2, 2
జవాబు:
C) 2, 2, 3
6. పొడి సున్నానికి నీటిని కలిపి తడి సున్నం తయారుచేయటం ఈ రకమైన చర్య.
A) రసాయన వియోగం
B) ఉష్ణమోచక చర్య
C) ఉష్ణగ్రాహక చర్య
D) రసాయన స్థానభ్రంశం
జవాబు:
B) ఉష్ణమోచక చర్య
7. టపాసులు పేలడం అనునది. ఈ రకమైన చర్య
A) క్షయకరణం
B) భంజనము
C) ఆక్సీకరణం
D) గాల్వనైజేషన్
జవాబు:
C) ఆక్సీకరణం
8. ఒక ప్రయోగంలో విడుదల అయిన ఒక వాయువు మండుచున్న పుల్లను ఇంకా ప్రకాశవంతంగా మండించిన ఆ వాయువు ……….
A) ఆక్సిజన్
B) నైట్రోజన్
C) హైడ్రోజన్
D) కార్బన్ డై ఆక్సైడ్
జవాబు:
A) ఆక్సిజన్
9. Zn + 2 HCl → ZnCl2 + H2 అనే రసాయన చర్య కింది వాటిలో దేనికి ఉదాహరణ? ఏది?
A) రసాయన సంయోగం
B) రసాయన వియోగం
C) రసాయన స్థానభ్రంశం
D) రసాయన ద్వంద్వ వియోగం
జవాబు:
C) రసాయన స్థానభ్రంశం
10. పొడి సున్నాన్ని నీటికి కలిపితే జరిగే చర్య ఒక …………
A) స్థానభ్రంశ చర్య
B) వాయువు విడుదల చేయు చర్య
C) ఉష్ణం విడుదల చేయు చర్య
D) దహన చర్య
జవాబు:
C) ఉష్ణం విడుదల చేయు చర్య
11. 4 మోల్ల హైడ్రోజన్ వాయువుతో చర్యలో పాల్గొని 4 మోల్ల నీటిని ఏర్పరచడానికి కావలసిన ఆక్సిజన్ వాయువు మోల్ల సంఖ్య
A) 1 మోల్
B) 2 మోల్లు
C) 3 మోలు
D) 4 మోలు
జవాబు:
B) 2 మోల్లు
12.

A) రసాయన సంయోగ చర్యలు
B) రసాయన వియోగ చర్యలు
C) రసాయన స్థానభ్రంశ చర్యలు
D) గ్వంద్వ వియోగ చర్యలు
జవాబు:
B) రసాయన వియోగ చర్యలు
13. క్రింది వాటిలో సరియైన తుల్య సమీకరణము
A) NaOH + Zn → NaZnO2 + H2
B) 2NaOH + Zn → Na2ZnO2 + H2
C) 2NaOH + 2Zn → 2NaZnO2 + H2
D) NaOH + 2Zn → NaZn2O2 + H2
జవాబు:
B) 2NaOH + Zn → Na2ZnO2 + H2
14. సిల్వర్ బ్రోమైడ్ రంగు……
A) ఎరుపు
B) నీలం
C) ఆకుపచ్చ
D) లేత పసుపు
జవాబు:
D) లేత పసుపు
![]()
15. ఆక్సీకరణం అనగా ………
A) ఆక్సిజన్ కలపటం
B) హైడ్రోజన్ తొలగించటం
C) ఎలక్ట్రానులను పోగొట్టుకొనుట
D) ఉష్ణవహన చర్య
జవాబు:
D) ఉష్ణవహన చర్య
16. క్షయకరణం అనగా ……
A) ఆక్సిజన్ కోల్పోవటం
B) హైడ్రోజన్ కలపటం
C) ఎలక్ట్రానులను గ్రహించుట
D) పైవన్నీ
జవాబు:
D) పైవన్నీ
17. రసాయన వియోగానికి ఈ క్రింది వాటిలో అవసరమైనది
A) కాంతి
B) ఉష్ణం
C) విద్యుత్
D) పైవన్నీ
జవాబు:
D) పైవన్నీ
18. ఈ క్రింది వానిలో ఆక్సీకరణానికి ఉదాహరణ
A) ఇనుము తుప్పుపట్టుట
B) శ్వాసక్రియ
C) ర్యాన్సిడిటీ
D) పైవన్నీ
జవాబు:
D) పైవన్నీ
19. ఈ క్రింది వాటిలో ఆక్సీకరణ చర్యకు ఉదాహరణ
A) కోసిన ఆపిల్ ముక్కలు రంగు మారటం
B) టపాసులు పేలటం
C) బంగాళదుంపల ముక్కలు రంగు మారటం
D) పైవన్నీ
జవాబు:
D) పైవన్నీ
20. రాన్సిడిటీని అరికట్టడానికి ఈ క్రింది వానిలో ఏది కలపాలి?
A) విటమిన్ సి
B) విటమిన్ ఇ
C) యాంటీ ఆక్సిడెంట్లు
D) పైవన్నీ
జవాబు:
D) పైవన్నీ
21. ఈ క్రింది వానిలో రసాయన మార్పు
A) బల్బు వెలగటం
B) ఇనుప ముక్క అయస్కాంతాన్ని ఆకర్షించటం
C) ఆహారం జీర్ణం అవటం
D) లోహాలు వ్యాకోచించటం
జవాబు:
D) లోహాలు వ్యాకోచించటం
22. ఈ క్రింది వానిలో భౌతిక మార్పు
A) పండ్లు పండటం
B) అగ్గిపుల్ల మండటం
C) సిమెంట్ గట్టి పడటం
D) నీరు ఆవిరిగా మారటం
జవాబు:
D) నీరు ఆవిరిగా మారటం
23. చర్యాశీలతలో భేదాల వలన జరుగు రసాయన చర్యలు
A) రసాయన సంయోగం
B) రసాయన వియోగం
C) స్థానభ్రంశం
D) ద్వంద్వ వియోగం
జవాబు:
C) స్థానభ్రంశం
24. శక్తిని బయటకు విడుదల చేసే చర్య …..
A) ఉష్ణమోచక
B) ఉష్ణగ్రాహక
C) ఉష్ణవినిమయ
D) ఉష్ణవహన
జవాబు:
A) ఉష్ణమోచక
25. శక్తిని గ్రహించే చర్య
A) ఉష్ణ మోచక
B) ఉష్ణగ్రాహక
C) ఉష్ణవినిమయ చర్య
D) పెవన్నీ
జవాబు:
B) ఉష్ణగ్రాహక
26. ఈ క్రింది వానిలో ఉష్ణగ్రాహక చర్యకు ఉదాహరణ
A) C + O2 → CO2 + Q
B) C + O2 → CO2 – Q
C) C + O2 + Q → CO2
D) పైవన్నీ
జవాబు:
A) C + O2 → CO2 + Q
27. ఈ క్రింది వానిలో ఉష్ణమోచక చర్యకు ఉదాహరణ
A) C + O2 → CO2 + Q
B) C + O2 → CO2 – Q
C) C + O2 + Q → CO2
D) B మరియు C
జవాబు:
D) B మరియు C
![]()
28. కూరగాయలు కంపోస్టుగా వియోగం చెందడం ……………. కు ఉదాహరణ.
A) ఆక్సీకరణము
B) క్షయకరణము
C) ముక్కిపోవడం
D) క్షయము చెందుట
జవాబు:
A) ఆక్సీకరణము
29. ఒక రసాయన చర్యలో ఉష్ణం గ్రహించబడి క్రొత్త పదార్థం ఏర్పడటాన్ని ……………… అంటారు.
A) ఉష్ణరసాయన చర్య
B) ఉష్ణమోచక చర్య
C) ఉష్ణగ్రాహక చర్య
D) కాంతిరసాయన చర్య
జవాబు:
C) ఉష్ణగ్రాహక చర్య
30. 2N2O → 2N2 + O ……………….. చర్యకు ఉదాహరణ.
A) రసాయన సంయోగ
B) రసాయన వియోగం
C) రసాయన స్థానభ్రంశ
D) రసాయన ద్వంద్వవియోగ
జవాబు:
D) రసాయన ద్వంద్వవియోగ
31. Ca + 2H2O → Ca(OH)2 + H2 ↑ అనేది ……………… చర్యకు ఉదాహరణ.
A) రసాయన సంయోగం
B) రసాయన వియోగం
C) రసాయన స్థానభ్రంశం
D) రసాయన ద్వంద్వ వియోగం
జవాబు:
C) రసాయన స్థానభ్రంశం
32. రసాయన సమీకరణంలో బాణం గుర్తుకు ఎడమవైపు ఉన్న పదార్థాలను ………….. అంటారు.
A) క్రియాజనకాలు
B) క్రియాజన్యాలు
C) అవక్షేపాలు
D) వాయువులు
జవాబు:
A) క్రియాజనకాలు
33. ఆపిల్, బంగాళదుంపలలో ఉండే ఎంజైమ్ …….
A) టయలిన్
B) పాలిఫినాల్ ఆక్సిడేజ్
C) టైరోసినేజ్
D) B మరియు C
జవాబు:
D) B మరియు C
34. వెండి, రాగి వస్తువులు మెరుపును కోల్పోవటాన్ని …………….. అంటారు.
A) ముక్కిపోవడం
B) తుప్పుపట్టడం
C) కుళ్ళిపోవడం
D) క్షయము చెందడం
జవాబు:
D) క్షయము చెందడం
35. ఇనుప వస్తువులపై జింక్ పూత వేయడాన్ని ………… అంటారు.
A) రాన్సిడేషన్
B) ఆక్సిడేషన్
C) రిడక్షన్
D) గాల్వనీకరణము
జవాబు:
D) గాల్వనీకరణము
36. తుప్పును నిరోధించే సామర్థ్యం గల లోహము …….
A) ఇనుము
B) బంగారం
C) ఉక్కు
D) రాగి
జవాబు:
B) బంగారం
37. ఆహారం పాడవకుండా నిల్వ ఉండుటకు ………….. విటమిన్లు కలపాలి.
A) విటమిన్ A & C
B) A & B విటమిన్
C) విటమిన్ C & E
D) విటమిన్ D & E
జవాబు:
C) విటమిన్ C & E
38. చిప్స్ తయారీదారులు, ఎక్కువకాలం నిల్వ ఉండడానికి ప్యాకెట్ లోపల …………. వాయువును నింపుతారు.
A) ఆక్సిజన్
B) నైట్రోజన్
C) హైడ్రోజన్
D) క్లోరిన్
జవాబు:
B) నైట్రోజన్
39. ముక్కిపోవటం ఒక ………… చర్య.
A) ఉష్ణమోచక
B) ఉష్ణగ్రాహక
C) ఆక్సీకరణ
D) క్షయకరణ
జవాబు:
C) ఆక్సీకరణ
40. Na → Na+ +e–. ఈ చర్యలో సోడియం ……………. చెందింది.ణ.
A) ఆక్సీకరణం
B) క్షయకరణం
C) రసాయన మార్పు
D) భౌతిక మార్పు
జవాబు:
A) ఆక్సీకరణం
41. Cl + e– → Cl– ఈ చర్యలో క్లోరిన్ ……. చెందింది.
A) ఆక్సీకరణం
B) క్షయకరణం
C) రసాయన మార్పు
D) భౌతిక మార్పు
జవాబు:
B) క్షయకరణం
![]()
42. NaOH + HCl → NaCl + H2O. ఇది …………… చర్యకు ఉదాహరణ.
A) రసాయన సంయోగం
B) రసాయన స్థానభ్రంశం
C) రసాయన వియోగం
D) రసాయన ద్వంద్వ వియోగం
జవాబు:
D) రసాయన ద్వంద్వ వియోగం
43. Fe+ CuSO4 → FeSO4 + Cu లో ఎక్కువ చర్యా శీలత గల లోహం ……………..
A) Fe
B) Cu
C) S
D) O2
జవాబు:
A) Fe
44. ఆక్సీకరణం, క్షయకరణం ఒకేసారి జరిగే చర్యలను…………….. అంటారు.
A) ఆక్సీకరణ చర్య
B) క్షయకరణ చర్య
C) రెడాక్స్ చర్య
D) రసాయన వియోగం
జవాబు:
C) రెడాక్స్ చర్య
45. CuO + H2 → Cu + H2O. ఈ చర్యలో Cu0 …………….. చెందింది.
A) ఆక్సీకరణం
B) క్షయకరణం
C) మార్పు
D) క్షయము
జవాబు:
B) క్షయకరణం
46. అవక్షేపాలు ఏర్పడే చర్యలను …………….. చర్యలు అంటారు.
A) సంయోగ
B) వియోగ
C) స్థానభ్రంశ
D) ద్వంద్వ వియోగ
జవాబు:
D) ద్వంద్వ వియోగ
47. అధిక చర్యాశీలత గల లోహాలు, అల్ప చర్యాశీలత గల లోహాలను ……………… చెందిస్తాయి.
A) స్థానభ్రంశం
B) వియోగం
C) సంయోగం
D) ద్వంద్వ వియోగం
జవాబు:
A) స్థానభ్రంశం
48. విద్యుత్ విశ్లేషణలో ఏర్పడిన హైడ్రోజన్, ఆక్సిజన్ నిష్పత్తి …………
A) 1:2
B) 2:1
C) 3:2
D) 2:3
జవాబు:
B) 2:1
49. లెడ్ అయోడైడ్ అవక్షేపం రంగు ………
A) ఎరుపు
B) తెలుపు
C) పసుపు
D) జేగురు
జవాబు:
C) పసుపు
50. క్షయము చెందుట అనునది ……………. చర్య.
A) ఆక్సీకరణం
B) క్షయకరణం
C) రెడాక్స్
D) ఏదీకాదు
జవాబు:
A) ఆక్సీకరణం
51. Fe2O3 + 2Al → Al2O3 + 2 Fe ఈ చర్య దేనికి ఉదాహరణ?
A) రసాయన సంయోగం
B) రసాయన వియోగచర్య
C) రసాయన స్థానభ్రంశం
D) రసాయన ద్వంద్వవియోగం
జవాబు:
C) రసాయన స్థానభ్రంశం
52. లేత పసుపుపచ్చరంగులో ఉండే ఒక పదార్థమును సూర్య కాంతిలో ఉంచితే అది బూడిద రంగులోనికి మారుతుంది. అయితే తీసుకోబడిన పదార్థం ఏమిటి?
A) లెడ్ అయోడైడ్
B) పొటాషియం అయోడైడ్
C) సిల్వర్ బ్రోమైడ్
D) హైడ్రోజన్ క్లోరైడ్
జవాబు:
C) సిల్వర్ బ్రోమైడ్
53. రసాయనిక చర్యలో అవక్షేపమును సూచించుటకు ఉపయోగించు బాణపు గుర్తు
A) →
B) ↑
C) ↓
D) ←
జవాబు:
C) ↓
![]()
54. కాల్షియం హైడ్రాక్సైడ్ అనేది …………. ద్రావణం.
A) ఆమ్ల
B) క్షార
C) తటస్థ
D) ద్వంద్వ స్వభావ
జవాబు:
B) క్షార
55. జింక్ సల్ఫేట్ ద్రావణం గల పరీక్షనాళికలో శుభ్రమైన ఇనుపముక్కలు ఉంచినప్పుడు ఏమి జరుగుతుందనగా ………………….
A) ద్రావణం రంగును కోల్పోయి, ఇనుపముక్కలపై జింక పూత ఏర్పడుతుంది.
B) గ్రావణం ఆకుపచ్చ రంగులోకి మారి, ఇనుప ముక్కలపై జింకప్పత ఏర్పడును.
C) ద్రావణాన్ని, ఆకుపచ్చ రంగులోకి మార్చుతూ, ఇనుపముక్కలు ద్రావణంలో కరుగుతాయి.
D) ఎటువంటి చర్య జరుగదు.
జవాబు:
D) ఎటువంటి చర్య జరుగదు.
56. ఒక విద్యారి పరీక్షనాళికలో (Pb(NO3)2) లెడ్ నైట్రోజన్ వేసి వేడిచేసినాక అందులోనుండి విడుదల అయిన వాయువులు
A) NO2 O2
B) NO2, H2
C) NO2, N2
D) NO2, CO2
జవాబు:
A) NO2 O2
57. CaCO3 ని వేడి చేయగా ఏర్పడిన పదార్థాలు
A) CaO, CO2
B) CaCO3, H2O
C) CaO, H2O
D) Ca, CO3
జవాబు:
A) CaO, CO2
58. సోడియంను నీటిలో వేసినప్పుడు అందులో ‘టప్’ మని మండి శబ్దం చేయును. దీనికి కారణం
A) నైట్రోజన్ వాయువు విడుదల
B) ఉష్ణం విడుదల అయినందువల్ల
C) H2 వాయువు విడుదల అయి మండటంవల్ల
D) ఆక్సిజన్ విడుదల అవడం వల్ల
జవాబు:
C) H2 వాయువు విడుదల అయి మండటంవల్ల
59. రాగి వస్తువులపై ఆకుపచ్చని పూతకు కారణమైన పదార్థం
A) CuO
B) CuCl2
C) Cus
D) CuSO4
జవాబు:
A) CuO
60. రంగుగల వస్తువులను విరంజనం (రంగును కోల్నో యేలా చేయడం) చేయగల పదార్థం
A) తేమగల ఆక్సిజన్ వాయువు
B) తేమ గల క్లోరిన్ వాయువు
C) తేమగల నైట్రోజన్ వాయువు
D) తేమగల కార్బన్ డై ఆక్సైడ్ వాయువు
జవాబు:
B) తేమ గల క్లోరిన్ వాయువు
61. 1 గ్రామ్ మోలార్ ద్రవ్యరాశి గల ఏదైనా వాయువులోని అణువుల సంఖ్య
A) 6.02 × 1023
B) 6.02 × 1022
C) 3.01 × 1022
D) 3.01 × 1011
జవాబు:
A) 6.02 × 1023
62. లోహాలు, ఆమ్లాలతో చర్య జరిపినపుడు వెలువడు వాయువు
A) H2
B) O2
C) N2
D) CO2
జవాబు:
A) H2
63. జింక్, సజల హైడ్రోక్లోరిక్ ఆమ్లంతో చర్య జరిపినపుడు విడుదలయ్యే వాయువు దగ్గరకు మండుచున్న అగ్గిపుల్లని తెచ్చినపుడు టప్ అనే శబ్దంతో అగ్గిపుల్ల ఆరిపోతుంది. వెలువడిన వాయువు ఏమి?
A) ఆక్సిజన్
B) హైడ్రోజన్
C) కార్బన్ డై ఆక్సైడ్
D) క్లోరిన్
జవాబు:
B) హైడ్రోజన్
64. ఒక రసాయన చర్య జరిగినపుడు విడుదలయ్యే వాయువు దగ్గరకు మండుచున్న అగ్గిపుల్లను తెచ్చినపుడు అగ్గిపుల్ల ప్రకాశవంతంగా మండుచున్నది. వెలువడిన వాయువు ఏది?
A) హైడ్రోజన్
B) కార్బన్ డై ఆక్సైడ్
C) ఆక్సిజన్
D) నైట్రోజన్
జవాబు:
C) ఆక్సిజన్
![]()
65. ఒక రసాయన చర్య జరిగినపుడు విడుదలయ్యే వాయువు దగ్గరకు మండుచున్న అగ్గిపుల్లను తెచ్చినపుడు అగ్గిపుల్ల ఆరిపోతుంది. అయితే వెలువడిన వాయువు ఏది?
A) కార్బన్ డై ఆక్సైడ్
B) హైడ్రోజన్
C) ఆక్సిజన్
D) నైట్రోజన్
జవాబు:
A) కార్బన్ డై ఆక్సైడ్
66. క్రింది రసాయన సమీకరణాలను పరిశీలించుము
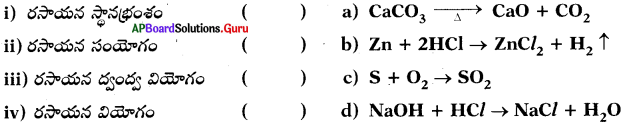
పైన ఇచ్చిన జతలకు క్రింది వానిలో సరియైన దానిని ఎంపిక చేయుము.
A) a, b, c, d
B) a, c, d, b
C) b, c, d, a
D) b, d, c, a
జవాబు:
C) b, c, d, a
II. జతపరచుము.
i)
| గ్రూప్ – ఎ | గ్రూప్ – బి |
| 1. ఆపిల్ | A) మిటమిన్ సి, ఇ |
| 2. చిప్స్ ప్యాకెట్లు | B) ర్యాన్సిడిటీ |
| 3. ఎక్కువ కాలం నిల్వ ఉండే ఆహార పదార్థాలు | C) క్రోజన్ |
| 4. మెరుపు కోల్పోవటం | D) నైట్రోజన్ వాయువు |
| 5. రుచి, వాసన మారిపోవటం | E) టైరోసినేజ్ |
జవాబు:
| గ్రూప్ – ఎ | గ్రూప్ – బి |
| 1. ఆపిల్ | E) టైరోసినేజ్ |
| 2. చిప్స్ ప్యాకెట్లు | D) నైట్రోజన్ వాయువు |
| 3. ఎక్కువ కాలం నిల్వ ఉండే ఆహార పదార్థాలు | A) మిటమిన్ సి, ఇ |
| 4. మెరుపు కోల్పోవటం | C) క్రోజన్ |
| 5. రుచి, వాసన మారిపోవటం | B) ర్యాన్సిడిటీ |
ii)
| గ్రూప్ – ఎ | గ్రూప్ – బి |
| 1. శక్తి గ్రహించటం | A) క్షయకరణం |
| 2. శక్తి విడుదల | B) ఆక్సీకరణం |
| 3. హైడ్రోజన్ కలుపుట | C) ఉష్ణగ్రాహక చర్య |
| 4. ఆక్సిజన్ కలుపుట | D) అవక్షేపం |
| 5. నీటిలో కరగని పదార్థాలు | E) ఉష్ణమోచక చర్య |
జవాబు:
| గ్రూప్ – ఎ | గ్రూప్ – బి |
| 1. శక్తి గ్రహించటం | C) ఉష్ణగ్రాహక చర్య |
| 2. శక్తి విడుదల | E) ఉష్ణమోచక చర్య |
| 3. హైడ్రోజన్ కలుపుట | A) క్షయకరణం |
| 4. ఆక్సిజన్ కలుపుట | B) ఆక్సీకరణం |
| 5. నీటిలో కరగని పదార్థాలు | D) అవక్షేపం |